恐惧和压抑等情绪反应是我们生活中对消极情况的正常心理和生理反应。频繁的急性情绪反应是一种病理状态,被称为慢性应激。长期的慢性应激压力会导致大脑中的各种神经变化,增加抑郁和焦虑的风险。精神疾病与免疫功能障碍密切相关,除了行为改变,慢性应激还会导致免疫代谢和心血管系统的紊乱。目前的研究已经发现了多种免疫因子在心理疾病中的生理功能,但仍不清楚外周T细胞在慢性应激诱导焦虑行为中的具体角色,如T细胞在慢性应激下有何种变化;心理疾病中病理T细胞的特征是什么;这种病理性T细胞通过何种机制调节中枢神经系统神经元活动。
2019年10月31日,威廉(中国)靳津实验室联合东南大学柴人杰实验室在Cell杂志发表了题为“Stress-induced metabolic disorder in peripheral CD4+ T cells leads to anxiety-like behavior”的研究论文,揭示了CD4+ T细胞嘌呤合成代谢功能紊乱与慢性应激诱导的心理疾病之间的联系。
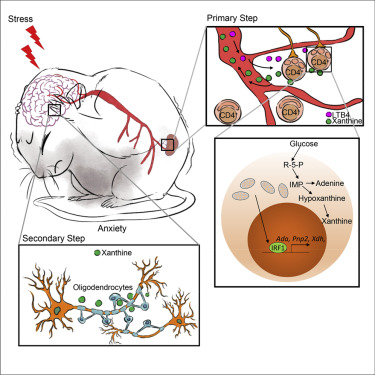
在该工作中,利用多种动物行为学实验作为评价标准,靳津团队发现体内缺少CD4+ T细胞的小鼠可以避免因外界压力下的慢性应激诱导产生心理疾病。实验数据显示,在慢性应激状态下,小鼠体内白三烯b4(LTB4)含量上升,使包括Naive T细胞在内的非炎性CD4+ T细胞线粒体分裂。代谢组学和转录组分析表明,CD4+ T细胞中线粒体分裂可导致转录因子IRF1累积,IRF1与Ada、Xdh和Pnp2启动子区结合促使葡萄糖更多的通过戊糖磷酸途径代谢,进而从头合成黄嘌呤。慢性应激焦虑模型中,小鼠血清黄嘌呤含量有显著的上升。临床证据也表明焦虑症患者与健康对照组相比血清黄嘌呤水平升高。大量的研究发现大脑杏仁核在恐惧与焦虑的产生中起着关键作用。压力状态下,CD4+T细胞产生的过量嘌呤(包括次黄嘌呤和黄嘌呤)通过血液循环进入脑部,与脑左侧杏仁核中少突胶质细胞上的腺苷受体A1结合,引起少突胶质细胞活化并增殖,继而过度活化左侧杏仁核区域神经元导致焦虑症状。
该研究成果确定了慢性应激如何影响外周CD4+ T细胞的线粒体形态,进而诱导产生的焦虑行为中的分子机制。临床治疗精神疾病的大多数药物直接针对中枢神经系统,而靶向其他系统干预精神疾病的药物或治疗手段有限。该工作加深对神经发育、精神疾病与免疫生理功能之间联系的理解,对了解抑郁症和焦虑症的发病机制并开发新的治疗药物具有重要意义。
靳津课题组博士研究生范柯琪与李异媛博士为文章的共同第一作者;浙江大学靳津教授与东南大学柴人杰教授为该论文的共同通讯作者。该课题得到了科技部重大专项、基金委优秀青年科学基金、浙江省杰出青年科学基金、中国科学院先导专项、国家自然科学基金面上项目的资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S0092867419311171